国内首个rhTSH上市申请获得CDE受理
今日,智核生物宣布,其自主研发的重组人促甲状腺素注射液(SNA001)已向中国国家药品监督管理局药品审评中心(CDE)提交生物制品许可申请(BLA)并获得受理,拟用于“无远处转移分化型甲状腺癌患者在甲状腺全切或近全切术后碘[131I]清除残余甲状腺组织的治疗”。SNA001有望成为国内首个上市的重组人促甲状腺素(rhTSH),打破此药物在中国大陆地区空白二十余年的状态;同时这是智核生物在中国第一次递交BLA,意味着该公司作为创新核药Biotech公司在商业化进程中向前迈出了重要一步。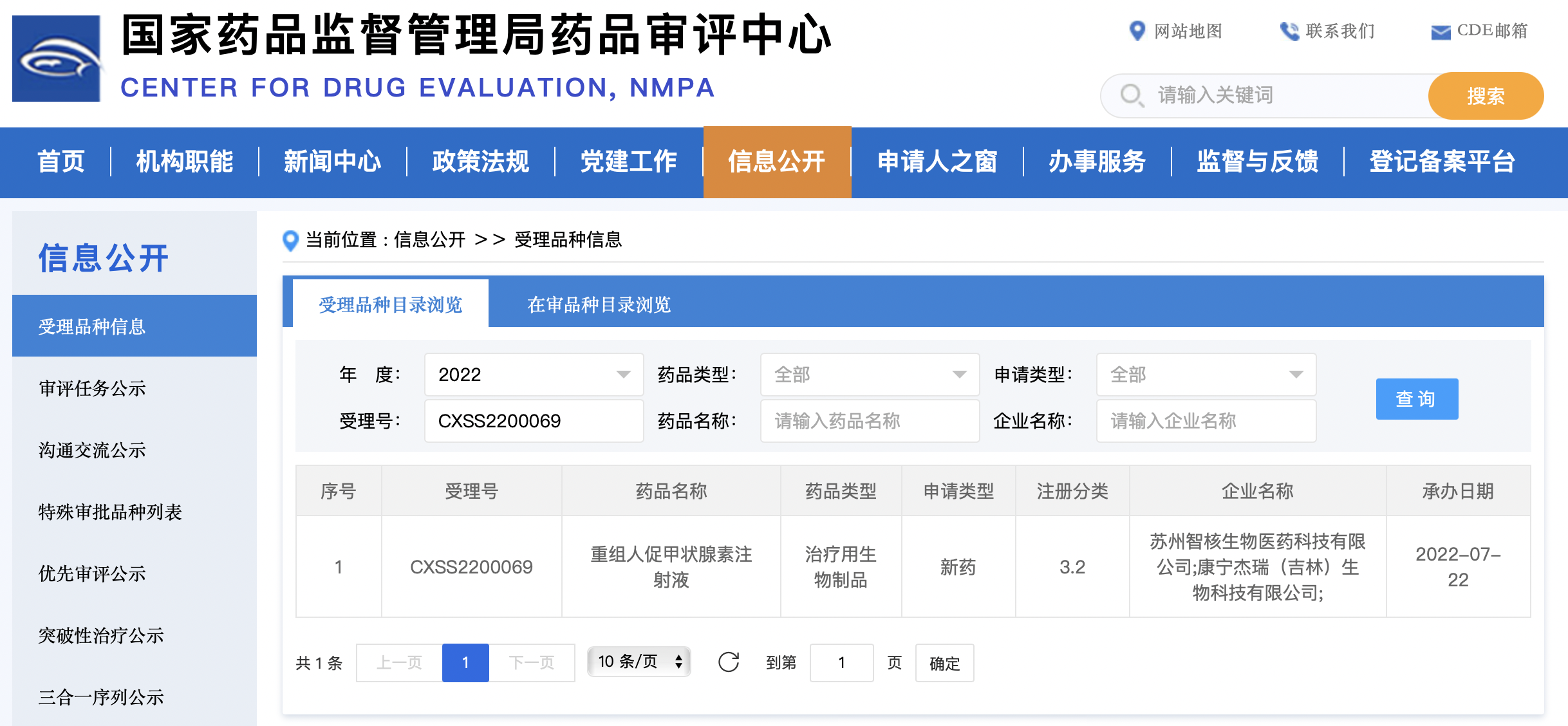
甲状腺癌流行病学及治疗金标准
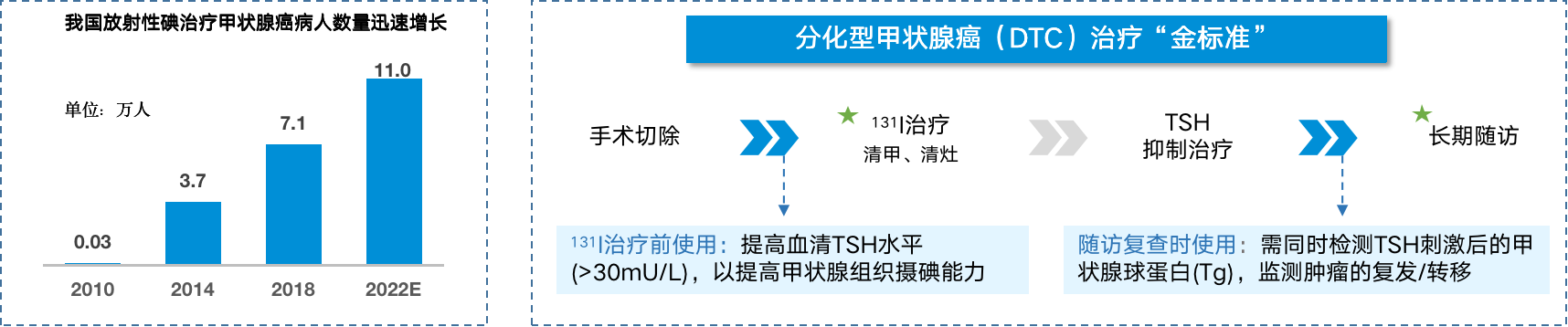
据全国肿瘤登记中心的数据显示,我国每年新发甲状腺癌病人约22万人,并以每年20%的速度持续增长。分化型甲状腺癌(DTC)占所有甲癌病例数的95%以上,虽总体死亡率较低,但仍处于增长态势。手术切除+TSH抑制治疗+131I治疗是目前国际公认的分化型甲状腺癌治疗的金标准,2020年接受131I治疗的DTC患者为8.4万人次,预计2022年将达到11万人次。
131I治疗甲状腺癌
131I治疗或随访复查前,均需要将病人血清TSH水平升高至30mU/L以上。提升TSH的方法有2种:一是传统的甲状腺激素撤退(THW),即停服甲状腺素3-4周,以提高内源性TSH的分泌;二是给予外源性TSH,即肌肉注射rhTSH。国内外多个指南强力推荐使用rhTSH作为停用甲状腺素的取代疗法,如《ATA甲状腺结节和分化型甲状腺癌治疗指南(2015版)》、《欧洲甲状腺学会(ETA)共识(2022版)》、中国肿瘤临床诊疗指南:《甲状腺癌诊疗指南(2022版)》、《131I治疗分化型甲状腺癌指南(2021版)》等。
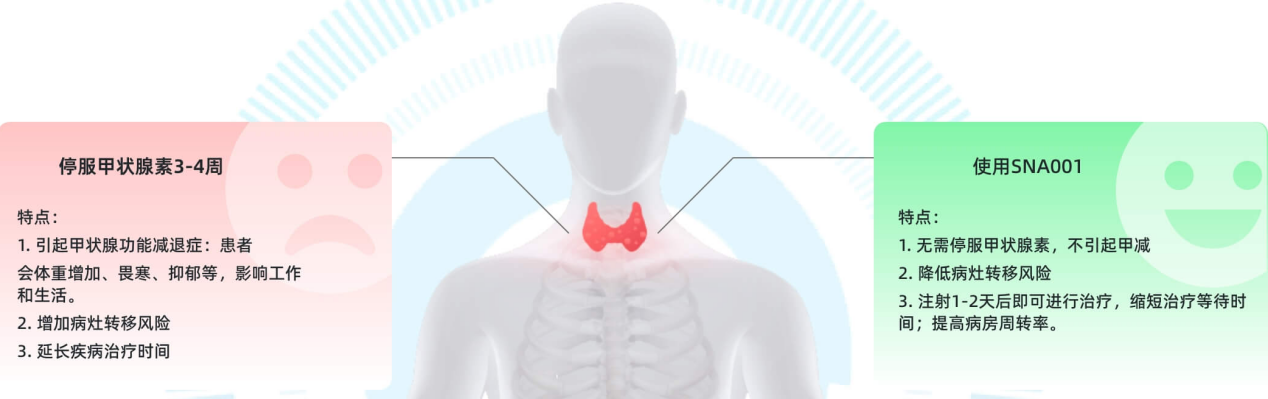
与THW方式相比,使用SNA001能够安全、快速提升血清TSH水平,仅需1-2天即可达到治疗要求,缩短治疗等待时间,还能够满足特殊患者的需求:即使停服甲状腺素后,体内TSH水平仍达不到治疗要求的患者。此外,选择rhTSH方式不需要停服甲状腺素,不会引起甲状腺功能减退如体重增加、畏寒、抑郁等不适症状,提高患者生活质量,最大程度的降低疾病复发的风险。

得知SNA001申报BLA已获得CDE受理的消息,中华医学会核医学分会副主任委员、复旦大学附属中山医院核医学科主任石洪成教授表示非常欣慰,石教授说:“我们见证了SNA001的每一步发展,2018年我们完成了临床I/II期试验,2019年我们作为组长单位启动了全国共计16家中心的Ⅲ期临床试验。现在我们希望SNA001能够尽快通过审批上市,打破国内甲状腺癌131I治疗无药可用的状态, 给临床及患者提供新的诊疗选择。”

中国核学会核医学分会理事长、中华医学会核医学分会前任主任委员李亚明教授也强调:“原研的rhTSH已在国外上市二十多年,造福广大的国外患者,而我们国内一直没有同类药物上市,很多DTC患者在131I治疗前只能选择THW方式,需要承受甲减的痛苦。智核生物正是从人文关怀角度让患者受益,极大减轻了部分不能耐受甲减患者的痛苦,充分体现了药物的价值。我们对SNA001充满期待,希望药物早日上市,造福国内的患者。”
智核生物创始人须涛博士表示:公司自创立之初就秉承“用最具创新性的核医学诊疗产品,给患者带来新的希望”的理念来研发药物,SNA001作为国内首个申报BLA的rhTSH,是以临床价值为导向、真正解决患者迫切需求的药物,我们期望药物能尽早获批,让更多的DTC患者拥有更好的诊疗方案。与此同时,我们自主研发的SNA002(68Ga标记PD-L1放射性显影剂)也已获得中美IND批准,接下来智核生物会全力加速,更早的为广大的肿瘤患者提供更加精准的核医学诊疗药物。
关于SNA001
SNA001由智核生物自主研发,其主要成分为重组人促甲状腺激素(rhTSH),是一种与天然人促甲状腺激素 (TSH) 相同的蛋白质。早期临床试验研究显示,该药物安全耐受性良好,与原研药物Thyrogen(赛诺菲)PK参数高度一致(Front Endocrinol. 2021 Feb 17)。2019年12月起,在全国16家研究中心开展 III期临床试验,累计纳入受试者307例。结果显示其疗效非劣效于目前临床实践中常用且唯一的THW 方法,且安全耐受性良好,具有明确的临床需求和价值。 此外,SNA001采用预充针剂型,工艺稳定,更易于临床操作。
关于智核生物
智核生物成立于2015年,是一家以“用最具创新性的核医学诊疗产品,给患者带来新的希望”为使命的核医药公司,致力于为全球患者提供创新性的放射性核素诊疗药物,产品覆盖甲状腺癌、肿瘤放射性核素诊断药物与治疗药物等领域。公司成立至今已获得4轮累计超过2亿元的风险投资。
智核生物创建了具有自主知识产权的基于单域抗体的放射性药物发现、研发、生产技术平台。公司前瞻性的布局了一系列专业化、高质量的放射性药物研发管线,涵盖10多个创新核素诊断和治疗产品,首个针对甲状腺癌放射性碘治疗的重组人促甲状腺激素(SNA001)新药上市申请已获得CDE受理,填补中国大陆131I治疗用药空白领域;多个创新的靶向肿瘤的放射性显影药物已经逐步进入临床,其中自主研发的放射性核素标记PD-L1的显影剂(SNA002)已获得中美IND双批准。
